РАЗДЕЛ ПЕРВЫЙ
ПРОВОДНИКОВЫЕ МАТЕРИАЛЫ И ИЗДЕЛИЯ
ГЛАВА Г.
ОСНОВНЫЕ СВОЙСТВА ПРОВОДНИКОВЫХ МАТЕРИАЛОВ
§ 1. Строение металлических проводниковых материалов
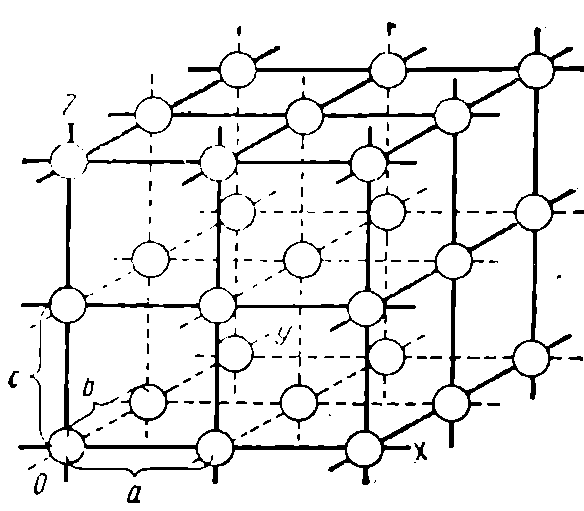
Рис. 1. Кубическая пространственная кристаллическая решетка
Металлические материалы (металлы) относятся к веществам, имеющим кристаллическое строение. Атомы кристаллических материалов располагаются друг относительно друга в строго определенном порядке по прямым линиям. Эти прямые линии, пересекаясь друг с другом, образуют пространственную решетку (рис. 1). В ней атомы занимают места пересечений прямых линий, называемых
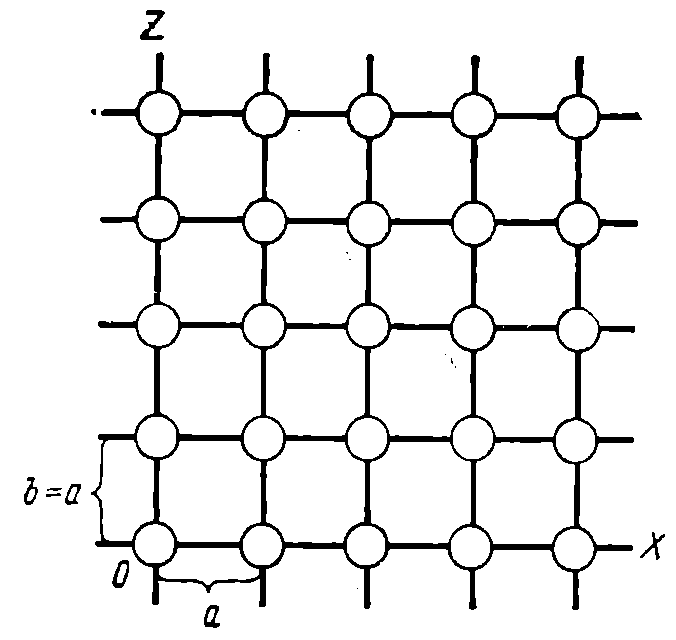
Рис. 2. Грань кубического кристалла
узлами кристаллической решетки. По каждому из трех направлений ox, оу, oz атомы располагаются на одинаковом расстоянии. Эти расстояния обозначаются буквами а, b, с и называются параметрами кристаллической решетки. Направления ох, су, oz называются кристаллографическими осями. Углы между кристалло-графическими осями у многих кристаллов прямые, но могут быть и непрямые.
Каждый кристалл представляет собой геометрическую фигуру, ограниченную плоскостями или гранями кристалла. Грани по расположению на них атомов подобны плоским сеткам.
На рис. 2 приведено изображение грани кубического кристалла.
Геометрическую форму кристаллической решетки, а следовательно, и вид кристалла определяют параметры а, b, с (см. рис. 1) и величины углов между кристаллографическими осями.
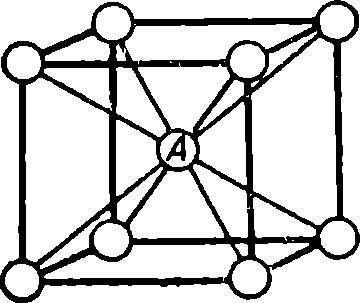
Рис. 3. Элементарная кристаллическая ячейка объемно-центрированного куба
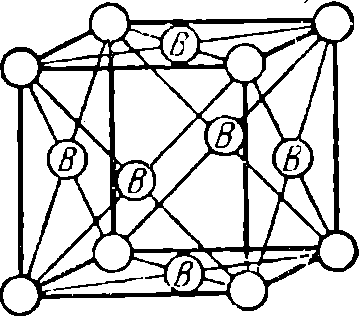
Рис. 4. Элементарная кристаллическая ячейка гранецентрированного куба
Если параметры а, b, с равны между собой, а углы между ними прямые, то кристаллическая решетка имеет форму куба и называется кубической. Если же параметры а, b, с не равны между собой, а углы между ними остались прямыми, то такую кристаллическую решетку называют призматической. Грани такого кристалла имеют форму прямоугольников.
Кроме кубической и призматической пространственных решеток для кристаллов возможны и другие геометрические фигуры. Основные металлические проводниковые, материалы, применяемые в электротехнических устройствах: медь Cu, железо Fe, алюминий Al, молибден Мо, вольфрам W и др. состоят из кристаллов, имеющих разные кубические решетки. Различают кубическую решетку, в центре которой располагается еще один атом А, и кубическую решетку, в центре каждой из шести граней которой находится еще по атому В. Первую называют объемно-центрированной кубической решеткой (рис. 3), а вторую — гранецентрированной кубической решеткой (рис. 4). Кристаллическую решетку объемно-центрированного куба имеют железо, вольфрам, хром, молибден и некоторые другие металлы, а гранецентрированный куб — медь, алюминий, никель, серебро и другие металлы. Следовательно, металл можно представить как вещество, состоящее из бесконечно большого количества атомов, расположенных в элементарных пространственных решетках. Во всех металлах наблюдаются небольшие отклонения от идеальных решеток — имеются незанятые узлы и некоторые смещения атомов.
Проводниковые материалы могут быть изготовлены из какого- либо одного чистого металла или из сплавов разных металлов. Если сплавляют два металла, то сплав называется двойным, если три — тройным и т. д. При изготовлении сплавов атомы одного металла могут входить в решетку другого, т. е. образовывать совместно с ним одну общую кристаллическую решетку. Такие сплавы называются твердыми растворами. При определенном количественном соотношении и резко отличающихся температурах плавления металлы могут не образовать твердого раствора, а микрокристаллизоваться каждый отдельно в виде самостоятельных зерен. И этом случае сплав будет механической смесью кристаллов исходных металлов. При сплавлении металла с металлом может образоваться и химическое соединение, кристаллическое строение которого будет отличным от строения исходных металлов.
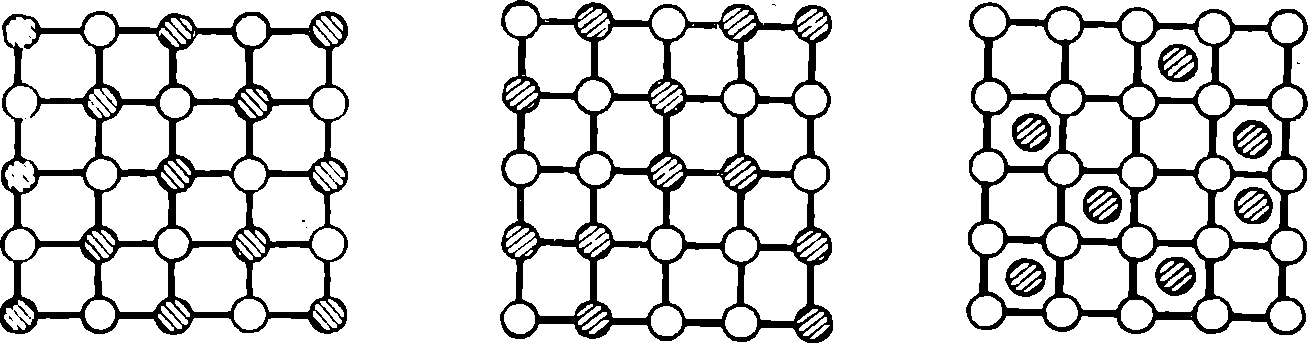
Рис. 7. Распределение атомов в решетке твердого раствора внедрения
Рис. 6. Распределение атомов в решетке твердого раствора неупорядоченного замещения
Рис. 5. Распределение атомов в решетке твердого раствора упорядоченного замещения
Сплавы в виде твердого раствора различаются между собой по тому, как располагаются в кристаллической решетке атомы сплавляемых металлов. Если атомы в общей решетке сплава располагаются с атомами другого, то такой сплав называют твердым раствором упорядоченного замещения. На рис. 5 показана плоская решетка такого сплава двух металлов. Если же атомы двух металлов в общей решетке сплава распределяются в ее узлах беспорядочно, то сплав называют твердым раствором неупорядоченного замещения (рис. 6). Твердый раствор, в котором кристаллическая решетка образуется из атомов одного какого-либо металла, а атомы второго внедряются в промежутки между ними, т. е. между узлами, получил название твердого раствора внедрения. Плоская решетка такого сплава изображена на рис. 7.
Итак, при сплавлении двух разных металлов или металла с неметаллом, например железа с углеродом, образуется новый материал в виде сплава. Сплавы имеют иную, чем исходные металлы, кристаллическую структуру, а следовательно, и иные механические и электрические свойства.
В сплавах при их образовании протекают сложные процессы кристаллизации. Каждый чистый металл имеет определенную температуру плавления, которая при охлаждении этого расплавленного металла является и температурой его кристаллизации. Если температура двух сплавляемых металлов превышает температуры плавления каждого из них, то они растворяются друг в друге. При охлаждении данного расплава кристаллизация начнется при одной температуре, а закончится при другой, более низкой.
t c
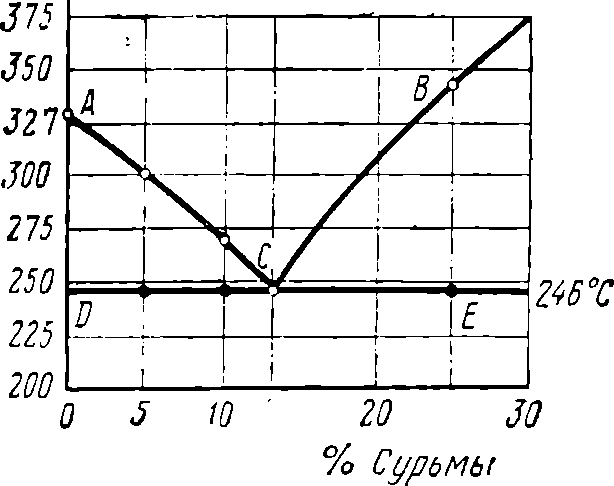
Рис. 8. Диаграмма состояния системы свинец — сурьма
Кристаллизация сплавов имеет температуру начала кристаллизации и температуру ее окончания. Для сплавов, имеющих различное содержание одних и тех же исходных металлов, эти температуры различны. Поэтому на диаграммах, в которых по вертикали наносятся величины температур, а по горизонтали — процентное содержание сплавляемых металлов (рис. 8), получаются две кривые. Линия АСВ, соответствующая температурам начала кристаллизации, получила название линии ликвидуса *, так как она является границей жидкого состояния всего сплава. Выше этой линии сплав находится в жидком состоянии. Линия DCE, соответствующая температурам окончания кристаллизации, называется линией солидуса**, так как она является начальной границей твердого состояния. Ниже этой линии сплав находится в твердом состоянии.
* Ликвидус (лат.) — жидкий, текущий.
**Солидус (лат.) — прочный.
Области диаграммы между двумя линиями (ACD и ВСЕ) содержат как твердый, так и жидкий растворы, т. е. в этих областях температур наблюдается два состояния сплава. Ниже линии солидуса сплав может представлять собой твердый раствор, химическое соединение сплавляемых металлов или их механическую смесь в зависимости от состава сплава и от других факторов. Рассмотренная диаграмма (рис. 8) называется диаграммой состояния сплавов системы свинец — сурьма (Pb — Sb). Эта диаграмма показывает, что начало затвердевания различных по составу сплавов свинца и сурьмы происходит при различных температурах, а окончание затвердевания — при одной определенной температуре (246°С). При содержании в сплаве 13% сурьмы (Sb) и 87% свинца (РЬ) кристаллизация сурьмы и свинца происходит одновременно при 246° С. При этом образуется механическая смесь металлов, называемая эвтектикой *, а сплав этого состава называется эвтектическим. Эвтектический сплав обладает самой низкой температурой плавления, что очень важно для практики.
Диаграммы состояния сплавов других металлов могут иметь другой вид, но и там имеются линии ликвидуса и солидуса.
*Эвтектика (греч.)— легкоплавящийся.


